近日,药学院姜虎林教授团队在权威期刊Advanced Materials上相继发表工程化干细胞用于组织纤维化治疗的一系列最新研究成果。
肺纤维化是一种进行性疾病,主要表现为呼吸系统损伤和肺组织功能修复障碍。肺血管生态位通过血管分泌因子在调节肺泡再生中起着至关重要的作用,然而肌成纤维细胞和血管内皮细胞之间的恶性串扰导致纤维化区域肺毛细血管的显著缺失,加剧肺纤维化进程。针对这一问题,该团队基于前期干细胞工程化技术(Sci Adv, 2020, 6: eaba3167;Sci Adv, 2023, 9: eadg5358)的基础上,开发了一种多功能工程化间充质干细胞(MSC-MM@LPHN),通过MSC膜表面锚定脂质聚合物纳米粒递送药物诱导肌成纤维细胞去分化,减少内皮细胞损伤因子的分泌,以及抑制血管内皮细胞向纤维化表型转化,从而恢复血管内皮细胞功能;同时结合MSC分泌生长因子促进血管生成作用,重塑纤维化区域正常血管结构,促进肺组织再生并逆转肺纤维化。
相关工作以“Engineered MSCs break endothelial-myofibroblast crosstalk in pulmonary fibrosis: reconstructing the vascular niche”为题发表在Advanced Materials上。中国药科大学药学院博士方月飞,硕士生张辰为本文的共同第一作者,中国药科大学周芳研究员、王广基院士和姜虎林教授为本文的共同通讯作者。
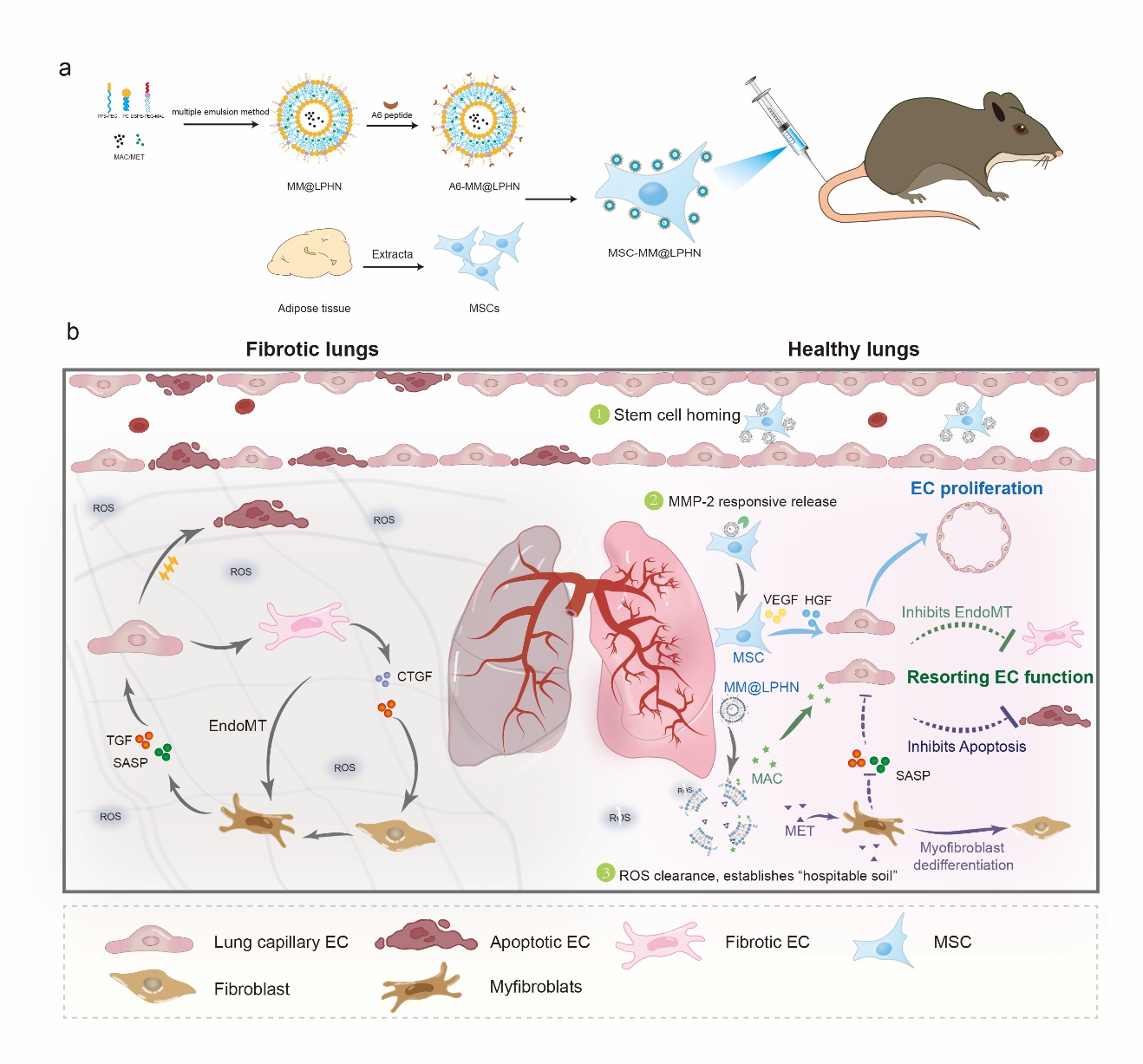
示意图
全文链接:https://advanced.onlinelibrary.wiley.com/doi/full/10.1002/adma.202414601
胰腺纤维化是慢性胰腺炎的独特组织病理学特征,表现为正常胰腺实质组织结构丧失,被纤维胶原取代。针对这类以组织修复为病症的疾病,通过具有自我更新、定向分化等功能的干细胞药物进行疾病干预是潜在的治疗手段。该团队前期发现干细胞用于纤维化治疗存在两大挑战:一是干细胞因其尺寸较大,在纤维胶原层的渗透能力受限,难以定向迁移到病灶深处(Adv Drug Deliv Rev. 2023; 200: 115051);二是纤维化的恶劣微环境造成干细胞在损伤部位迅速凋亡失活,削弱疗效(J Control Release. 2024; 365: 981-1003)。因此,该团队开发了一种一氧化氮脂质体嫁接的工程化MSC,通过调节胶原纤维缓解血管压迫,推动干细胞在胰腺组织分布并增强干细胞体内活性,提高治疗效果。
相关工作以“Engineered stem cell booster breakspathological barriers to treat chronic pancreatitis”为题发表在Advanced Materials上。中国药科大学理学院博士后韩涵,中国药科大学药学院硕士生陈比特、刘杨及东南大学医学院祁靓博士为本文的共同第一作者,延边大学附属医院心血管内科主任成宪武教授、中国药科大学/新疆医科大学黄张建教授、东南大学附属中大医院李玲教授及中国药科大学姜虎林教授为本文的共同通讯作者。

示意图
全文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202416261
据悉,该团队将进一步聚焦干细胞的工程化改造及其组织纤维化的应用治疗,积极推动研究开发向科技成果的落地转化。以上工作获得科技部重点研发计划项目、国家自然科学基金重点国际(地区)合作研究项目、江苏省前沿引领技术基础研究重大项目、长白山英才杰出团队项目以及中国药科大学多靶标天然药物全国重点实验室研究课题的资助。
(供稿单位:药学院,撰写人:刘华,审稿人:刘帆)





